Авторы: Michael Mitterberger, Wolfgang Horninger, Friedrich Aigner, Germar M. Pinggera, Ilona Steppan, Peter Rehder, and Ferdinand Frauscherb
Вступление
УЗИ является широко используемым и хорошо переносимым методом визуализации для оценки состояния простаты. Последние технические достижения в области ультразвуковых технологий привели к появлению новых аспектов в анализе предстательной железы. Структурный анализ применяется для измерения объема простаты, изучения эхотекстуры и иллюстрации жесткости или эластичности ткани. Функциональный анализ иллюстрирует макрососудистость и микрососудистость, которые являются показателями тканевой перфузии.
Анатомия простаты
Предстательная железа находится между шейкой мочевого пузыря и мочеполовой диафрагмой, чуть впереди прямой кишки. Железа традиционно описывается на основе патологической зональной архитектуры. Эти отделы состоят из передней фибромышечной стромы, которая лишена железистой ткани, переходной зоны, центральной зоны, периуретральной зоны и периферической зоны. Далее предстательная железа делится на вершину и основание (направлено вверх к нижней границе мочевого пузыря). Нормальная предстательная железа имеет размеры примерно 3 × 3 × 5 см или объем 25 мл. 70% рака простаты находятся в периферической зоне, тогда как 20% выходят из переходной зоны и 10% из центральной зоны. Нервно-сосудистый пучок протекает двусторонне вдоль заднелатерального аспекта простаты и является преимущественным путем распространения опухоли.
Предстательная железа производит и выделяет щелочную жидкость, которая заряжает и защищает сперму во время эякуляции. Обычно простата изменяется и увеличивается с возрастом. Простатит, доброкачественная гиперплазия предстательной железы (ДГПЖ) и рак предстательной железы (РПЖ) являются наиболее распространенными типами заболеваний предстательной железы. РПЖ является наиболее распространенным злокачественным новообразованием у мужчин. Трансректальное ультразвуковое исследование (ТРУИ) является широко используемым методом визуализации для оценки простаты. Преимущества ТРУИ по сравнению с другими методами – это низкая стоимость, хорошая доступность и возможность визуализации простаты в реальном времени.
Острый и хронический простатит
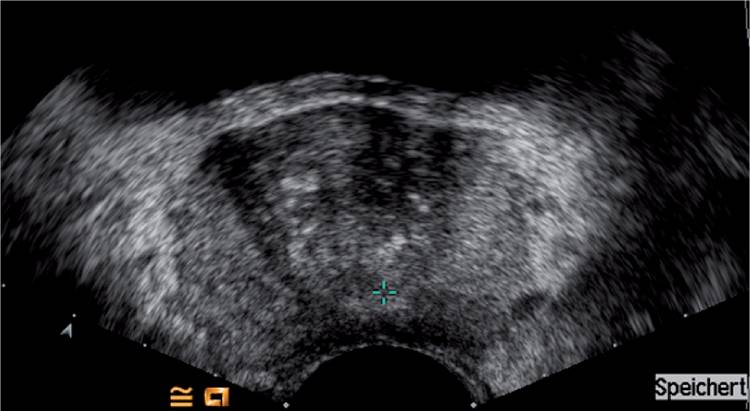
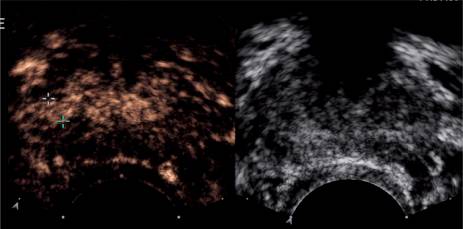
Распространенность простатита колеблется от 5% до 11%. Простатит встречается в любом возрасте, и его частота увеличивается с годами. Острый бактериальный простатит часто начинается с озноба и лихорадки, дискомфорта в животе, боли в промежности и жжения при мочеиспускании. При хроническом бактериальном простатите (когда симптомы сохраняются в течение не менее 3 месяцев) боль в промежности и увеличение частоты болезненного мочеиспускания являются наиболее распространенными симптомами. Острый или хронический бактериальный простатит с подтвержденной или предполагаемой инфекцией следует отличать от синдрома хронической тазовой боли (СХТБ) в соответствии с классификацией, предложенной Национальным институтом диабета и заболеваний органов пищеварения и почек. Патофизиология простатита не совсем понятна. У пациентов с простатитом активность простатического антибактериального фактора снижается, а рН очень щелочной. Бактерии (чаще всего Escherichia coli) проникают в предстательную железу путем восходящей уретральной инфекции, рефлюкса инфицированной мочи в протоки предстательной железы или лимфатического / гематогенного распространения. Острый бактериальный простатит на УЗИ представлен в виде гипоэхогенного ободка вокруг простаты, а цветное допплеровское изображение показывает усиление кровотока (Рис. 1). Абсцесс предстательной железы выглядит сонографически как гипоэхогенная линия жидкости. При хроническом бактериальном простатите можно обнаружить диффузное усиление контрастного вещества. Контрастные агенты показывают повышенную перфузию предстательной железы во время острой и хронической инфекции, однако они не используются в обычной клинической практике, так как никаких исследований по этой проблеме не проводилось.
Рисунок 1: Снимок простаты у 55-летнего мужчины с уровнем ПСА 3,25 нг / мл без подозрительной области.
Доброкачественная гиперплазия предстательной железы
Более 32 миллионов мужчин во всем мире имеют симптомы, связанные с ДГПЖ, и ДГПЖ поражает более 50% мужчин в возрасте старше 60 лет и до 90% мужчин в возрасте старше 70 лет. ДГПЖ представляет собой доброкачественное заболевание предстательной железы и состоит из узловой гиперплазии фиброзной, мышечной и железистой ткани в периуретральной и переходной зонах. Точная патофизиология ДГПЖ до сих пор неизвестна, но, вероятно, она связана с гормональными изменениями, которые происходят с возрастом у мужчин. ДГПЖ во время ТРУИ выглядит как эхогенная и неподвижная масса. ТРУИ в основном используется для оценки объема простаты, что имеет решающее значение для терапевтических стратегий. Объем простаты может быть оценен последовательной планиметрией, ортогональной плоскостью, вращательным телом (одиночная плоскость, эллипсоид) и трехмерными методами. Предполагается, что поэтапная планиметрия является наиболее точным методом определения объема простаты, но она требует много времени и громоздкого специального оборудования. Одномерные измерения предпочтительнее в клинике. Формула вытянутого эллипсоида, умножает наибольший переднезадний (высота), поперечный (ширина) и цефалокаудальный (длина) диаметры предстательной железы на 0,524 (В × Ш × Д × π / 6), вероятно, является наиболее часто используемым методом, поскольку он быстрый, воспроизводимый, и было показано, что имеет высокую корреляцию с фактическим объемом простаты.
Рак простаты
РПЖ является наиболее распространенным злокачественным заболеванием среди мужчин в западных странах. Кроме того, РПЖ обычно протекает бессимптомно на ранней стадии, и большинство видов рака локализуются в периферической зоне. У пациентов с повышенными значениями простат-специфического антигена (ПСА) подозревается РПЖ, и поэтому проводится цифровое ректальное исследование и биопсия под руководством ТРУИ. Визуализация играет центральную роль в выявлении, локализации и постановке пациентов с РПЖ.
Трансректальная визуализация
Использование режима серой шкалы ТРУИ все еще является руководством для биопсии простаты. Классический РПЖ выглядит на ТРУИ как гипоэхогенный узелок, однако это было в эпоху, предшествующую ПСА. В настоящее время из-за низких предельных значений ПСА РПЖ обнаруживается на более ранней стадии, и многие очаги рака кажутся изоэхогенными и, следовательно, не могут быть обнаружены с помощью серой шкалы.
В результате скрининга ПСА с низкими пороговыми значениями произошла поэтапная миграция в сторону менее агрессивного, ограниченного органами рака. Стадия чувствительности в исследованиях с использованием серой шкалы варьировала от 30% до 50% с специфичностью от 77% до 96%. Трехмерное ТРУИ помогло в оценке экстракапсулярного расширения и инвазии семенного пузырька.
Трансректальная цветная допплеровская визуализация
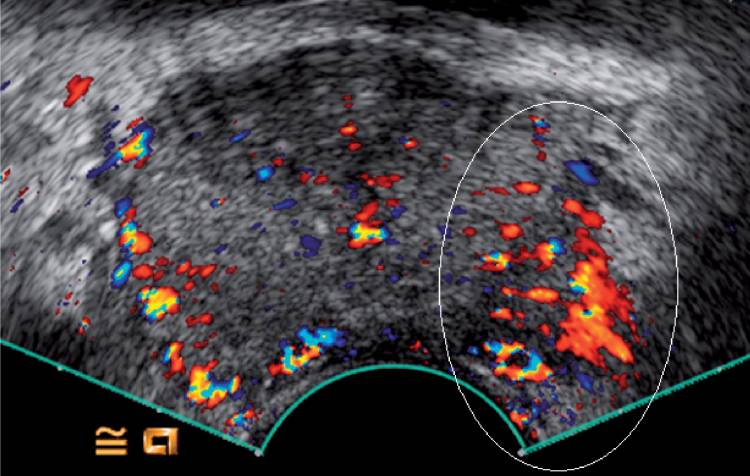
Цветная допплеровская визуализация хорошо известна для изображение макрососудистости и, следовательно, перфузии. РПЖ имеет повышенную плотность микрососудов по сравнению со здоровой тканью предстательной железы. Следовательно, доплеровская визуализация кровотока в сосудистой сети может помочь в обнаружении и локализации РПЖ (Рис. 2). Кроме того, степень рака положительно коррелирует со степенью доплеровского сигнала. В других исследованиях сравнивали систематические биопсии под допплерографическим контролем с достижением уровня обнаружения до 40%.
Рисунок 2: Допплерография с усилением цвета демонстрирует явно большее усиление левой стороны (белый эллипсоид). Целевая биопсия подтвердила наличие очага рака, Глисон 3 + 4.
Трансректальная допплерография с контрастным усилением
УЗИ с контрастом можно использовать для иллюстрации макрососудистости и микрососудистости. Микропузырьки с липидной или галактозной оболочкой, заполненной инертным газом, диаметром 1–10 мкм вводят внутривенно. Эти микропузырьки могут быть использованы в качестве усилителя сигнала для УЗИ, что приводит к визуализации кровотока в микрососудах. Новые контрастные вещества постоянно разрабатываются. Наиболее широко используемыми ультразвуковыми агентами при РПЖ являются Левовист (Schering, Германия) и SonoVue (Бракко, Италия). Для обнаружения контрастного вещества могут применяться несколько различных методов приема сигналов.
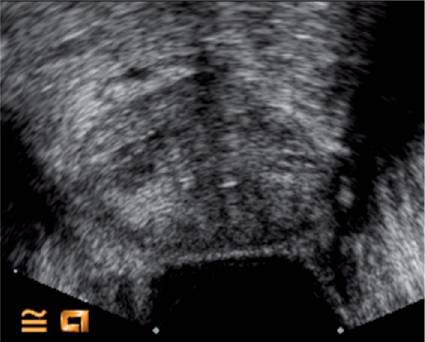
Рисунок 3: Снимки в режиме серых шкал простаты у 57-летнего мужчины с уровнем ПСА 4,8 нг / мл без подозрительной области.
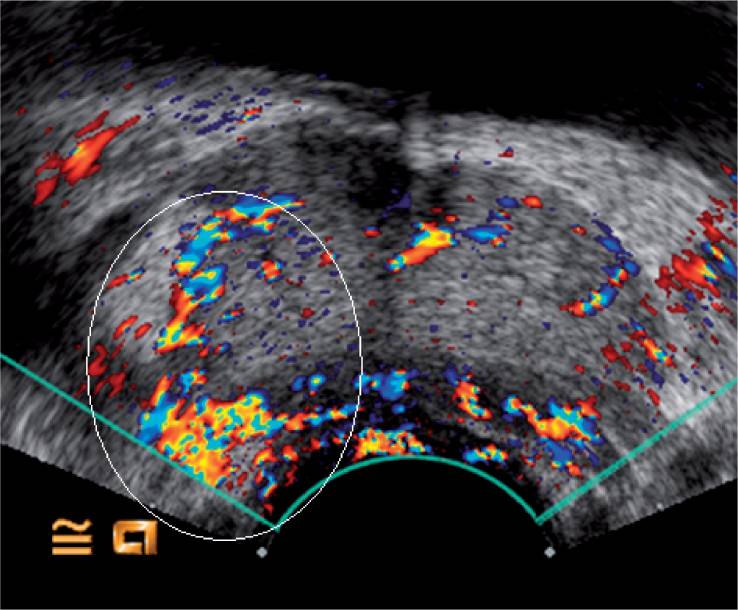
Рисунок 4: Допплерография с усилением цвета демонстрирует явно большее усиление правой стороны (белый эллипсоид). Целевая биопсия подтвердила наличие очага рака, Глисон 3 + 4.
Трансректальные контрастно-специфические методы УЗИ
Разработка специфических УЗИ методик использования контрастных веществ открыла новый потенциал в обнаружении микрососудистости. Эти методы используют нелинейные свойства контрастных веществ и, следовательно, обеспечивают лучшее осевое и пространственное разрешение.
Халперн и др. оценивали обнаружение РПЖ и распознавание доброкачественных образований из ткани злокачественной простаты с контрастным УЗИ с использованием непрерывной гармонической визуализации и прерывистой гармонической визуализации, а также непрерывного цветового и энергетического допплера. Целевые очаги биопсии были получены из мест наибольшего усиления. РПЖ был обнаружен в 363 очагах биопсии у 104 из 301 субъекта (35%). РПЖ был обнаружен в 15,5% (175 из 1133) целевых очагов и в 10,4% (188 из 1806) секстантных очагов (P <0,01). Авторы пришли к выводу, что частота обнаружения РПЖ в участках с усиленной контрастностью значительно выше по сравнению с ядрами-секстантами. Контрастная трансректальная сонография с прерывистой гармонической визуализацией обеспечивает статистически значимое улучшение разграничения между доброкачественными и злокачественными участками биопсии. Однако, учитывая относительно низкие рабочие характеристики датчика, этот метод может оказаться недостаточным для прогнозирования того, какие пациенты имеют доброкачественные и злокачественные заболевания.
Новые методы ультразвуковой визуализации были разработаны, чтобы лучше отделить информацию от эхо-пузырьков и тканей. Отображение последовательности импульсов каденции и контраста (CPS) – это многоимпульсный метод с низким энергопотреблением, при котором импульсы с различной амплитудой и фазой передаются, а полученные эхо-сигналы суммируются. Эта последовательность визуализации приводит к существенному подавлению ткани, что позволяет обнаруживать присутствие небольшого количества контрастных веществ, сохраняемых в ткани. Кроме того, CPS можно использовать с низким механическим индексом для предотвращения разрушения пузырьков, что является обязательным требованием для последовательной визуализации целевых контрастных агентов (Рис. 5).
Рисунок 5: Снимки предстательной железы у 60-летнего мужчины с уровнем ПСА 7,4 нг / мл. Никаких отклонений не наблюдалось при визуализации (с правой стороны). Каденция контрастно-импульсного секвенирования (CPS) показывает быстро усиливающееся поражение (через 18 с после введения болюса) с правой стороны (между перекрестными линиями). Усиление сильнее, чем в оставшейся ткани простаты. Три из пяти целевых очагов были положительными на рак.
Эластография в режиме реального времени
Другой недавно внедренный метод – эластография в режиме реального времени (RTE), которая позволяет продемонстрировать распределение эластичности ткани в одном УЗИ срезе. Этот многообещающий метод рассчитывается с помощью алгоритмов постобработки и не требует контрастного вещества. Таким образом, RTE – это метод, который показывает разные области с разной жесткостью в цветном кодированном изображении одновременно с B-режимом или режимом серых шкал. RTE находилась на стадии исследований в течение многих лет, но только недавно приблизилась к клинической практике, и в различных опубликованных исследованиях появляется все больше доказательств того, что RTE еще больше улучшит обнаружение РПЖ.
Сперандео и др. сообщили о пользе визуализации эластичности для дифференциации злокачественных и доброкачественных поражений. Они использовали эластичность ткани для выявления рака на основе деформации ткани при ручном сжатии предстательной железы трансректальным датчиком. Сумура и др. сравнивали эластограммы с патологическими данными образцов простатэктомии. Они сообщили, что уровень обнаружения опухолей даже объемом менее 1 мл составлял 73% и составлял 100% для опухолей объемом более 5 мл. Они также сообщили, что частота выявления опухолей, расположенных в задней части железы (74%), была почти равна частоте выявления опухолей в передней части (75%).
Саломон и др. использовали эластографию для определения чувствительности и специфичности выявления РПЖ у пациентов, которым назначена радикальная простатэктомия. 109 пациентов с подтвержденной биопсией локализованного РПЖ подверглись эластографии перед радикальной простатэктомией. Они обнаружили чувствительность и специфичность для обнаружения РПЖ 75,4% и 76,6% соответственно. (Рис. 6 и Рис. 7).
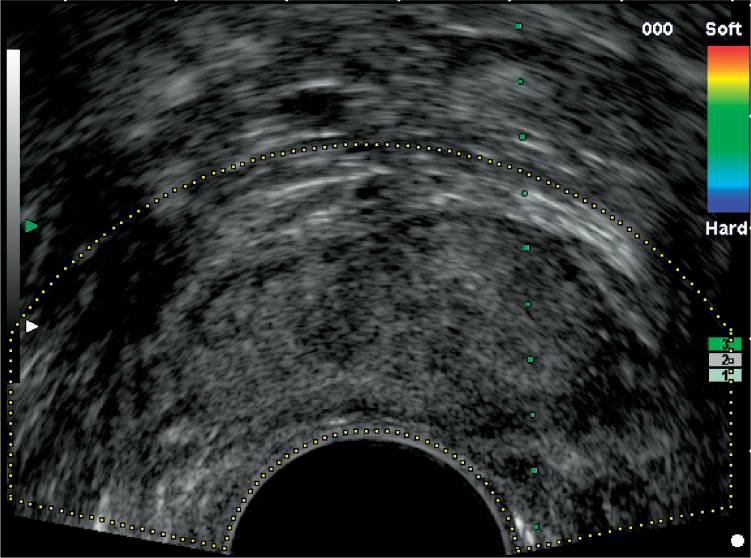
Рисунок 6: Поперечное трансректальное изображение простаты без четких доказательств рака предстательной железы.
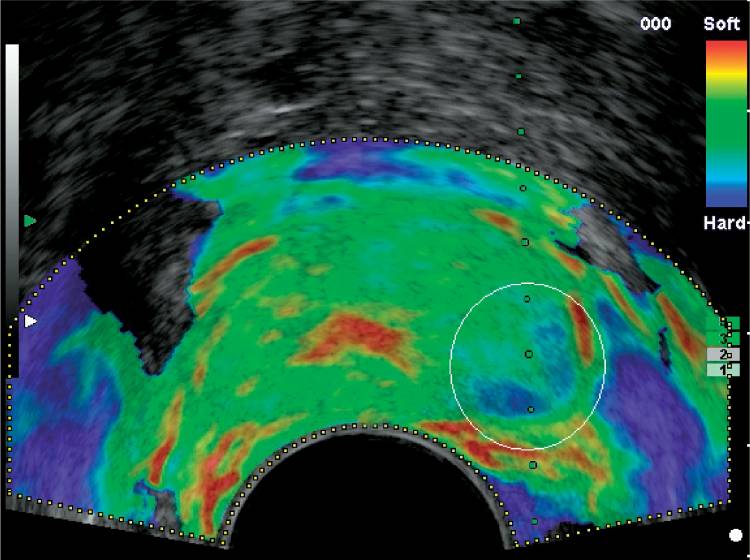
Рисунок 7: Соответствующее эластографическое изображение простаты. Эластограмма показывает четко видимую более жесткую область (синего цвета) с подозрением на рак простаты на левой стороне предстательной железы (белая точка).
Итог
Трансректальная биопсия простаты под УЗИ контролем с минимальным количеством 10 биопсийных очагов периферической зоны остается золотым стандартом для обнаружения РПЖ в случае повышенного уровня ПСА. Эластографически направленная биопсия с контрастным усилением или в реальном времени может значительно увеличить обнаружение РПЖ. УЗИ с контрастным усилением позволяет обнаруживать значительно более высокий балл по шкале Глисона, что важно для оценки РПЖ. Эластография в реальном времени, по-видимому, предлагает новый потенциал в постановке РПЖ по сравнению с результатами радикальной простатэктомии. Кроме того, новые контрастные методы могут улучшить диагностику РПЖ и даже избежать ненужных биопсий в будущем.